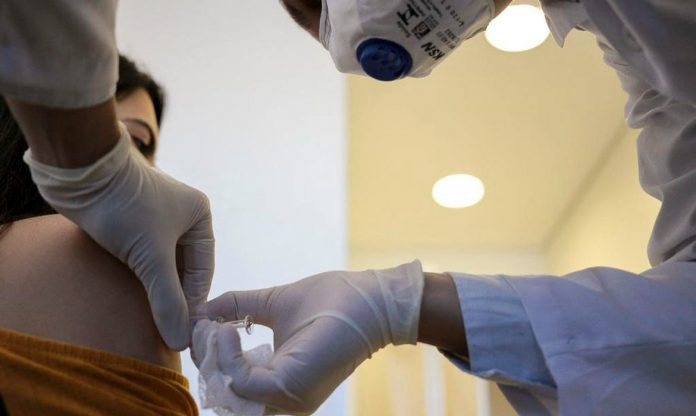
A primeira ‘submissão contínua’ de uma vacina contra COVID-19, que está sendo desenvolvida pela AstraZeneca em colaboração com a Universidade de Oxford, foi entregue para a Anvisa para revisão. Portanto, a parte técnica da Agência começou a avaliar o este primeiro pacote de dados, que é referente aos estudos não clínicos.
Entretanto, ainda é cedo para afirmar que a análise sobre a qualidade da vacina foi concluída. Afinal, diversos dados precisam ser submetidos a estudos ainda. Além disso, o procedimento vai permitir que a Anvisa tenha mais agilidade na solicitação de autorização da vacina no Brasil.

Como funciona este processo?
Normalmente, todos os dados sobre a eficácia, segurança e qualidade de um medicamento e demais documentos devem ser apresentados no início da avaliação em um pedido formal de registro.
Neste caso, a Anvisa irá analisar os dados à medida em que se tornam disponíveis. As consultas podem ser realizadas por meio do site: https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2020/covid-19-novo-modo-de-submissao-para-analise-de-vacina.
Além disso, os ensaios clínicos em grande escala, que envolvem milhares de pessoas estão em andamento e o Brasil participa de um desses estudos. No entanto, a ‘submissão contínua’ continuará até que evidências suficientes estejam disponíveis para suportar um pedido formal de registro e após a avaliação pela empresa quanto à suficiência dos dados de qualidade, eficácia e segurança para o estabelecimento de uma relação de benefício-risco positiva e robusta, considerando a indicação terapêutica pleiteada e as discussões prévias com a Anvisa.





















